Химические свойства щелочноземельных металлов и их соединений. Щелочные и щелочноземельные металлы. с неметаллами IV–VI групп
К щелочноземельным металлам относятся металлы IIa группы: бериллий, магний, кальций, стронций, барий и радий. Отличаются легкостью, мягкостью и сильной реакционной способностью.
Общая характеристика
От Be к Ra (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств, реакционная способность. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns 2:
- Be - 2s 2
- Mg - 3s 2
- Ca - 4s 2
- Sr - 5s 2
- Ba - 6s 2
- Ra - 7s 2
Природные соединения
В природе щелочноземельные металлы встречаются в виде следующих соединений:
- Be - BeO*Al 2 O 3 *6SiO 2 - берилл
- Mg - MgCO 3 - магнезит, MgO*Al 2 O 3 - шпинель, 2MgO*SiO 2 - оливин
- Ca - CaCO 3 - мел, мрамор, известняк, кальцит, CaSO 4 *2H 2 O - гипс, CaF 2 - флюорит

Получение
Это активные металлы, которые нельзя получить электролизом раствора. С целью их получения применяют электролиз расплавов, алюминотермию и вытеснением их из солей другими более активными металлами.
MgCl 2 → (t) Mg + Cl 2 (электролиз расплава)
CaO + Al → Al 2 O 3 + Ca (алюминотермия - способ получения металлов путем восстановления их оксидов алюминием)
MgBr 2 + Ca → CaBr 2 + Mg

Химические свойства

Оксиды щелочноземельных металлов
Имеют общую формулу RO, например: MgO, CaO, BaO.
Получение
Оксиды щелочноземельных металлов можно получить путем разложения карбонатов и нитратов:
MgCO 3 → (t) MgO + CO 2
Ca(NO 3) 2 → (t) CaO + O 2 + NO 2
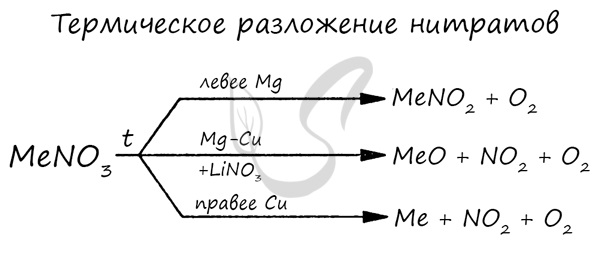
Химические свойства
Проявляют преимущественно основные свойства, все кроме BeO - амфотерного оксида.

Гидроксиды щелочноземельных металлов
Проявляют основные свойства, за исключением гидроксида бериллия - амфотерного гидроксида.
Получение
Получают гидроксиды в реакции соответствующего оксида металла и воды (все кроме Be(OH) 2)
CaO + H 2 O → Ca(OH) 2
Химические свойства
Основные свойства большинства гидроксидов располагают к реакциям с кислотами и кислотными оксидами.
Ba(OH) 2 + H 2 SO 4 → BaSO 4 ↓ + H 2 O
Ca(OH) 2 + H 2 O + CO 2 → Ca(HCO 3) 2 + H 2 O
Ca(HCO 3) 2 + Ca(OH) 2 → CaCO 3 + H 2 O + CO 2
Ca(OH) 2 + CO 2 → CaCO 3 ↓ + H 2 O

Реакция с солями (и не только) идут в том случае, если соль растворимы и по итогам реакции выделяется газ, выпадает осадок или образуется слабый электролит (вода).
Ba(OH) 2 + Na 2 SO 4 → BaSO 4 ↓ + NaOH
Гидроксид бериллия относится к амфотерным: проявляет двойственные свойства, реагируя и с кислотами, и с основаниями.
Be(OH) 2 + HCl → BeCl 2 + H 2 O
Be(OH) 2 + NaOH → Na 2
Жесткостью воды называют совокупность свойств воды, зависящая от присутствия в ней преимущественно солей кальция и магния: гидрокарбонатов, сульфатов и хлоридов.
Различают временную (карбонатную) и постоянную (некарбонатную) жесткость.

Вероятно, вы часто устраняете жесткость воды у себя дома, осмелюсь предположить - каждый день. Временная жесткость воды устраняется обычным кипячением воды в чайнике, и известь на его стенках - CaCO 3 - бесспорное доказательство устранения жесткости:
Ca(HCO 3) 2 → CaCO 3 ↓ + CO 2 + H 2 O
Также временную жесткость можно устранить, добавив Na 2 CO 3 в воду:
Ca(HCO 3) 2 + Na 2 CO 3 → CaCO 3 ↓ + NaHCO 3
С постоянной жесткостью бороться кипячением бесполезно: сульфаты и хлориды не выпадут в осадок при кипячении. Постоянную жесткость воды устраняют добавлением в воду Na 2 CO 3:
CaCl 2 + Na 2 CO 3 → CaCO 3 ↓ + NaCl
MgSO 4 + Na 2 CO 3 + H 2 O → 2 CO 3 ↓ + CO 2 + Na 2 SO 4
Жесткость воды можно определить с помощью различных тестов. Чрезмерно высокая жесткость воды приводит к быстрому образованию накипи на стенках котлов, труб, чайника.

©Беллевич Юрий Сергеевич
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к
IIA группа содержит только металлы – Be (бериллий), Mg (магний), Ca (кальций), Sr (стронций), Ba (барий) и Ra (радий). Химические свойства первого представителя этой группы — бериллия — наиболее сильно отличаются от химических свойств остальных элементов данной группы. Его химические свойства во многом даже более схожи с алюминием, чем с остальными металлами IIA группы (так называемое «диагональное сходство»). Магний же по химическим свойствами тоже заметно отличается от Ca, Sr, Ba и Ra, но все же имеет с ними намного больше сходных химических свойств, чем с бериллием. В связи со значительным сходством химических свойств кальция, стронция, бария и радия их объединяют в одно семейство, называемое щелочноземельными металлами .
Все элементы IIA группы относятся к s -элементам, т.е. содержат все свои валентные электроны на s -подуровне. Таким образом, электронная конфигурация внешнего электронного слоя всех химических элементов данной группы имеет вид ns 2 , где n – номер периода, в котором находится элемент.
Вследствие особенностей электронного строения металлов IIA группы, данные элементы, помимо нуля, способны иметь только одну единственную степень окисления, равную +2. Простые вещества, образованные элементами IIA группы, при участии в любых химических реакциях способны только окисляться, т.е. отдавать электроны:
Ме 0 – 2e — → Ме +2
Кальций, стронций, барий и радий обладают крайне высокой химической активностью. Простые вещества, образованные ими, являются очень сильными восстановителями. Также сильным восстановителем является магний. Восстановительная активность металлов подчиняется общим закономерностям периодического закона Д.И. Менделеева и увеличивается вниз по подгруппе.
Взаимодействие с простыми веществами
с кислородом
Без нагревания бериллий и магний не реагируют ни с кислородом воздуха, ни с чистым кислородом ввиду того, что покрыты тонкими защитными пленками, состоящими соответственно из оксидов BeO и MgO. Их хранение не требует каких-либо особых способов защиты от воздуха и влаги, в отличие от щелочноземельных металлов, которые хранят под слоем инертной по отношению к ним жидкости, чаще всего керосина.
Be, Mg, Ca, Sr при горении в кислороде образуют оксиды состава MeO, а Ba – смесь оксида бария (BaO) и пероксида бария (BaO 2):
2Mg + O 2 = 2MgO
2Ca + O 2 = 2CaO
2Ba + O 2 = 2BaO
Ba + O 2 = BaO 2
Следует отметить, что при горении щелочноземельных металлов и магния на воздухе побочно протекает также реакция этих металлов с азотом воздуха, в результате которой, помимо соединений металлов с кислородом, образуются также нитриды c общей формулой Me 3 N 2 .
с галогенами
Бериллий реагирует с галогенами только при высоких температурах, а остальные металлы IIA группы — уже при комнатной температуре:
Мg + I 2 = MgI 2 – иодид магния
Са + Br 2 = СаBr 2 – бромид кальция
Ва + Cl 2 = ВаCl 2 – хлорид бария
с неметаллами IV–VI групп
Все металлы IIA группы реагируют при нагревании со всеми неметаллами IV–VI групп, но в зависимости от положения металла в группе, а также активности неметаллов требуется различная степень нагрева. Поскольку бериллий является среди всех металлов IIA группы наиболее химически инертным, при проведении его реакций с неметаллами требуется существенно бо льшая температура.
Следует отметить, что при реакции металлов с углеродом могут образовываться карбиды разной природы. Различают карбиды, относящиеся к метанидам и условно считающимися производными метана, в котором все атомы водорода замещены на металл. Они так же, как и метан, содержат углерод в степени окисления -4, и при их гидролизе или взаимодействии с кислотами-неокислителями одним из продуктов является метан. Также существует другой тип карбидов – ацетилениды, которые содержат ион C 2 2- , фактически являющийся фрагментом молекулы ацетилена. Карбиды типа ацетиленидов при гидролизе или взаимодействии с кислотами-неокислителями образуют ацетилен как один из продуктов реакции. То, какой тип карбида – метанид или ацетиленид — получится при взаимодействии того или иного металла с углеродом, зависит от размера катиона металла. С ионами металлов, обладающих малым значением радиуса, образуются, как правило, метаниды, с ионами более крупного размера – ацетилениды. В случае металлов второй группы метанид получается при взаимодействии бериллия с углеродом:
Остальные металлы II А группы образуют с углеродом ацетилениды:
С кремнием металлы IIA группы образуют силициды — соединения вида Me 2 Si, с азотом – нитриды (Me 3 N 2), фосфором – фосфиды (Me 3 P 2):
с водородом
Все щелочноземельные металлы реагируют при нагревании с водородом. Для того чтобы магний прореагировал с водородом, одного нагрева, как в случае со щелочноземельными металлами, недостаточно, требуется, помимо высокой температуры, также и повышенное давление водорода. Бериллий не реагирует с водородом ни при каких условиях.
Взаимодействие со сложными веществами
с водой
Все щелочноземельные металлы активно реагируют с водой с образованием щелочей (растворимых гидроксидов металлов) и водорода. Магний реагирует с водой лишь при кипячении вследствие того, что при нагревании в воде растворяется защитная оксидная пленка MgO. В случае бериллия защитная оксидная пленка очень стойкая: с ним вода не реагирует ни при кипячении, ни даже при температуре красного каления:
c кислотами-неокислителями
Все металлы главной подгруппы II группы реагируют с кислотами-неокислителями, поскольку находятся в ряду активности левее водорода. При этом образуются соль соответствующей кислоты и водород. Примеры реакций:
Ве + Н 2 SO 4(разб.) = BeSO 4 + H 2
Mg + 2HBr = MgBr 2 + H 2
Ca + 2CH 3 COOH = (CH 3 COO) 2 Ca + H 2
c кислотами-окислителями
− разбавленной азотной кислотой
С разбавленной азотной кислотой реагируют все металлы IIA группы. При этом продуктами восстановления вместо водорода (как в случае кислот-неокислителей) являются оксиды азота, преимущественно оксид азота (I) (N 2 O), а в случае сильно разбавленной азотной кислоты – нитрат аммония (NH 4 NO 3):
4Ca + 10HNO 3( разб .) = 4Ca(NO 3) 2 + N 2 O + 5H 2 O
4Mg + 10HNO 3(сильно разб.) = 4Mg(NO 3) 2 + NН 4 NO 3 + 3H 2 O
− концентрированной азотной кислотой
Концентрированная азотная кислота при обычной (или низкой) температуре пассивирует бериллий, т.е. в реакцию с ним не вступает. При кипячении реакция возможна и протекает преимущественно в соответствии с уравнением:
Магний и щелочноземельные металлы реагируют с концентрированной азотной кислотой с образованием большого спектра различных продуктов восстановления азота.
− концентрированной серной кислотой
Бериллий пассивируется концентрированной серной кислотой, т.е. не реагирует с ней в обычных условиях, однако реакция протекает при кипячении и приводит к образованию сульфата бериллия, диоксида серы и воды:
Be + 2H 2 SO 4 → BeSO 4 + SO 2 + 2H 2 O
Барий также пассивируется концентрированной серной кислотой вследствие образования нерастворимого сульфата бария, но реагирует с ней при нагревании, сульфат бария растворяется при нагревании в концентрированной серной кислоте благодаря его превращению в гидросульфат бария.
Остальные металлы главной IIA группы реагируют с концентрированной серной кислотой при любых условиях, в том числе на холоду. Восстановление серы может происходить до SO 2 , H 2 S и S в зависимости от активности металла, температуры проведения реакции и концентрации кислоты:
Mg + H 2 SO 4( конц .) = MgSO 4 + SO 2 + H 2 O
3Mg + 4H 2 SO 4( конц .) = 3MgSO 4 + S↓ + 4H 2 O
4Ca + 5H 2 SO 4( конц .) = 4CaSO 4 +H 2 S + 4H 2 O
с щелочами
Магний и щелочноземельные металлы со щелочами не взаимодействуют, а бериллий легко реагирует как растворами щелочей, так и с безводными щелочами при сплавлении. При этом при осуществлении реакции в водном растворе в реакции участвует также и вода, а продуктами являются тетрагидроксобериллаты щелочных или щелочноземельных металлов и газообразный водород:
Be + 2KOH + 2H 2 O = H 2 + K 2 — тетрагидроксобериллат калия
При осуществлении реакции с твердой щелочью при сплавлении образуются бериллаты щелочных или щелочноземельных металлов и водород
Be + 2KOH = H 2 + K 2 BeO 2 — бериллат калия
с оксидами
Щелочноземельные металлы, а также магний могут восстанавливать менее активные металлы и некоторые неметаллы из их оксидов при нагревании, например:
Метод восстановления металлов из их оксидов магнием называют магниетермией.
Рассмотрим химические свойства щелочноземельных металлов. Определим особенности их строения, получения, нахождения в природе, применение.
Положение в ПС
Для начала определим расположение этих элементов в Менделеева. Они располагаются во второй группе главной подгруппе. К ним относят кальций, стронций, радий, барий, магний, бериллий. Все они на содержат по два валентных электрона. В общем виде бериллий, магний и щелочноземельные металлы на внешнем уровне имеют ns2 электронов. В химических соединениях они проявляют степень окисления +2. Во время взаимодействия с другими веществами они проявляют восстановительные свойства, отдавая электроны с внешнего энергетического уровня.
Изменение свойств
По мере возрастания ядра атома бериллий, магний и усиливают свои металлические свойства, так как наблюдается возрастание радиуса их атомов. Рассмотрим физические свойства щелочноземельных металлов. Бериллий в обычном состоянии является металлом серого цвета со стальным блеском. Он имеет плотную гексагональную кристаллическую решетку. При контакте с кислородом воздуха, бериллий сразу же образует оксидную пленку, в результате чего снижается его химическая активность, образуется матовый налет.
Физические свойства
Магний в качестве простого вещества является белым металлом, образующим на воздухе оксидное покрытие. Он имеет гексагональную кристаллическую решетку.
Физические свойства щелочноземельных металлов кальция, бария, стронция схожи. Они представляют собой металлы с характерным серебристым блеском, покрывающиеся под воздействием кислорода воздуха желтоватой пленкой. У кальция и стронция кубическая гранецентрированная решетка, барий имеет объемно-центрированную структуру.
Химия щелочноземельных металлов основывается на том, что у них металлический характер связи. Именно поэтому они отличаются высокой электрической и тепло проводимостью. Температуры их плавления и кипения больше, чем у щелочных металлов.

Способы получения
Производство бериллия в промышленных объемах осуществляется путем восстановления металла из фторида. Условием протекания данной химической реакции является предварительное нагревание.
Учитывая, что щелочноземельные металлы в природе находятся в виде соединений, для получения магния, стронция, кальция проводят электролиз расплавов их солей.

Химические свойства
Химические свойства щелочноземельных металлов связаны с необходимостью предварительного устранения с их поверхности слоя оксидной пленки. Именно она определяет инертность данных металлов к воде. Кальций, барий, стронций при растворении в воде образуют гидроксиды, имеющие ярко выраженные основные свойства.
Химические свойства щелочноземельных металлов предполагают их взаимодействие с кислородом. Для бария продуктом взаимодействия является пероксид, для всех остальных после реакции образуются оксиды. У всех представителей данного класса оксиды проявляют основные свойства, только для оксида бериллия характерны амфотерные свойства.
Химические свойства щелочноземельных металлов проявляются и в реакции с серой, галогенами, азотом. При реакциях с кислотами, наблюдается растворение данных элементов. Учитывая, что бериллий относится к амфотерным элементам, он способен вступать в химическое взаимодействие с растворами щелочей.

Качественные реакции
Основные формулы щелочноземельных металлов, рассматриваемые в курсе неорганической химии, связаны с солями. Для выявления представителей данного класса в смеси с другими элементами, можно использовать качественное определение. При внесении солей щелочноземельных металлов в пламя спиртовки, наблюдается окрашивание пламени катионами. Катион стронция дает темный красный оттенок, катион кальция - оранжевый цвет, а катион бария зеленый тон.
Для выявления катиона бария в качественном анализе используют сульфат анионы. В результате данной реакции образуется сульфат бария белого цвета, который нерастворим в неорганических кислотах.
Радий является радиоактивным элементом, который в природе содержится в незначительных количествах. При взаимодействии магния с кислородом, наблюдается ослепительная вспышка. Данный процесс некоторое время применяли во время фотографирования в темных помещениях. Сейчас на смену магниевым вспышкам пришли электрические системы. К семейству щелочноземельных металлов относится бериллий, который реагирует со многими химическими веществами. Кальций и магний аналогично алюминию, могут восстанавливать такие редкие металлы, как титан, вольфрам, молибден, ниобий. Данные называют кальциетермией и магниетермией.

Особенности применения
Каково применение щелочноземельных металлов? Кальций и магний используют для изготовления легких сплавов и редких металлов.
К примеру, магний содержится в составе дюралюминия, а кальций - это компонент свинцовых сплавов, используемых для получения оболочек кабелей и создания подшипников. Широко применение щелочноземельных металлов в технике в виде оксидов. (оксид кальция) и жженая магния (оксид магния) требуются для строительной сферы.
При взаимодействии с водой оксида кальция происходит выделение существенного количества теплоты. (гидроксид кальция) применяется для строительства. Белая взвесь данного вещества (известковое молоко) применяют в сахарной промышленности для процесса очистки свекловичного сока.

Соли металлов второй группы
Соли магния, бериллия, щелочноземельных металлов можно получить путем взаимодействия с кислотами их оксидов. Хлориды, фториды, иодиды данных элементов являются белыми кристаллическими веществами, в основном хорошо растворимыми в воде. Среди сульфатов растворимостью обладают только соединения магния и бериллия. Наблюдается ее снижение от солей бериллия к сульфатам бария. Карбонаты практически не растворяются в воде либо имеют минимальную растворимость.
Сульфиды щелочноземельных элементов в незначительных количествах содержатся в тяжелых металлах. Если направить на них освещение, можно получить различные цвета. Сульфиды включаются в состав светящихся составов, именуемых фосфорами. Применяют подобные краски для создания светящихся циферблатов, дорожных знаков.
Распространенные соединения щелочноземельных металлов
Карбонат кальция является самым распространенным на земной поверхности элементом. Он является составной частью таких соединений, как известняк, мрамор, мел. Среди них основное применение имеет известняк. Этот минерал незаменим в строительстве, считается отличным строительным камнем. Кроме того, из данного неорганического соединения получают негашеную и гашеную извести, стекло, цемент.
Применение известковой щебенки способствует укреплению дорог, а благодаря порошку можно снизить кислотность почвы. представляет собой раковины древнейших животных. Данное соединение используют для изготовления резины, бумаги, создания школьных мелков.
Мрамор востребован у архитекторов, скульпторов. Именно из мрамора были созданы многие уникальные творения Микеланджело. Часть станций московского метро облицована именно мраморными плитками. Карбонат магния в больших объемах используется при изготовлении кирпича, цемента, стекла. Он нужен в металлургической промышленности для удаления пустой породы.
Сульфат кальция, содержащийся в природе в виде гипса (кристаллогидрата сульфата кальция), применяется в строительной отрасли. В медицине данное соединение применяется для изготовления слепков, а также для создания гипсовых повязок.
Алебастр (полуводный гипс) при взаимодействии с водой выделяет огромное количество тепла. Это также применяется в промышленности.
Английская соль (сульфат магния) применяется в медицине в виде слабительного средства. Данное вещество обладает горьким вкусом, оно обнаружено в морской воде.
«Баритовая каша» (сульфат бария) не растворяется в воде. Именно поэтому данную соль применяют в рентгенодиагностике. Соль задерживает рентгеновские лучи, что позволяет выявлять заболевания желудочно-кишечного тракта.
В составе фосфоритов (горной породы) и апатитов есть фосфат кальция. Они нужны для получения соединений кальция: оксидов, гидроксидов.
Кальций играет для живых организмов особое значение. Именно этот металл необходим для построения костного скелета. Ионы кальция необходимы для регулировки работы сердца, повышения свертываемости крови. Недостаток его вызывает нарушения в работе нервной системы, потере свертываемости, утрате способности рук нормально держать различные предметы.
Для того чтобы избежать проблем со здоровьем, каждые сутки человек должен потреблять примерно 1,5 грамма кальция. Основная проблема заключается в том, что для того, чтобы организм усваивал 0,06 грамма кальция, необходимо съедать 1 грамм жира. Максимальное количество данного металла содержится в салате, петрушке, твороге, сыре.

Заключение
Все представители второй группы главной подгруппы таблицы Менделеева необходимы для жизни и деятельности современного человека. Например, магний является стимулятором обменных процессов в организме. Он должен присутствовать в нервной ткани, крови, костях, печени. Магний является активным участником и фотосинтеза у растений, так как он является составной частью хлорофилла. Кости человека составляют примерно пятую часть от общего веса. Именно в них содержится кальций и магний. Оксиды, соли щелочноземельных металлов нашли разнообразное применение в строительной сфере, фармацевтике и медицине.
Щелочноземельные металлы образуют основные оксиды, которые получают термическим разложением карбонатов или нитратов:
СаCO 3 = СаO + CO 2 ; 2Ba(NO 3) 2 = 2BaO + 4NO 2 + O 2
Энергично взаимодействуют с водой с образованием растворимых сильных оснований (щелочей).
При переходе от Ca(OH) 2 к Ba(OH) 2 растворимость заметно увеличивается (от 0,02 М до 0,2 М), в том же направлении увеличивается термическая устойчивость гидроксидов и усиливаются основные свойства. По силе основания уступают только гидроксидам щелочных металлов. Раствор Ва(ОН) 2 – баритовая вода – лабораторный реактив на CO 2 .
Катионы щелочноземельных металлов образуют соли со всеми кислотами. Хорошо растворимы галогениды, нитраты, перхлораты и большинство кислых солей. Плохо растворимы в воде фториды, карбонаты, силикаты и фосфаты. Образование мелкокристаллического осадка сульфата бария является качественной реакцией на сульфат-анион:
Ba 2+ + SO 4 2- = BaSO 4
Присутствие в природной воде растворимых солей кальция и магния обуславливает ее жесткость. Количественно жесткость измеряют суммарной концентрацией катионов Ca 2+ и Mg 2+ (ммоль экв/л). Различают временную (карбонатную) и постоянную жесткость. Первая удаляется кипячением:
Ca(HCO 3) 2 = CaCO 3 + CO 2 + H 2 O; Mg(HCO 3) 2 = Mg(OH) 2 + 2CO 2
Для удаления постоянной жесткости к воде добавляют вещества (соду, фосфат натрия и т.п.), переводящие катионы кальция и магния в осадок. Кроме того применяют метод ионного обмена, в этом случае катионы Ca 2+ и Mg 2+ меняются на катионы водорода или щелочного металла, удерживаемые на поверхности полимерной смолы (катионита).
Гидриды представляют собой белые солеподобные вещества, разлагающиеся водой с выделением водорода, сильные восстановители. В отличие от бериллия и магния, гидриды щелочноземельных металлов можно получить прямым синтезом:
Ca + H 2 = CaH 2
Литература: с. 587 - 599, с. 481 - 486, с. 447 - 460
7.4. Элементы ia-подгруппы (щелочные металлы)
Элементы IA-подгруппы: литий - Li, натрий - Na, калий - K, рубидий - Rb, цезий - Cs и радиоактивный франций часто называют щелочными металлами. Общая формула ns 1 обуславливает проявление щелочными металлами степени окисления +1.
Увеличение эффективного радиуса и уменьшение энергии ионизации в ряду Li – Na – K – Rb – Cs сопровождается заметным увеличением активности металлов. Небольшой радиус атома лития вызывает довольно сильные отличия данного элемента от остальных щелочных металлов, что в первую очередь проявляется в склонности к образованию ковалентных связей. Для натрия и особенно элементов подгруппы калия образование ковалентных связей нетипично. Малый размер и большая энергия гидратации катиона лития приводит к нарушению ожидаемой последовательности расположения щелочных металлов в ряду стандартных электродных потенциалов (литий стоит в нем первым). Нарушается ожидаемая последовательность активности щелочных металлов и в расплавах, в которых натрий более активен, что связано с образованием его ионом более прочных кристаллических решеток:
KOH + Na = NaOH + K
Литий, натрий, калий и рубидий - серебристо-белые металлы, цезий золотисто-желтого цвета. На воздухе поверхность лития, натрия и калия очень быстро тускнеет, рубидий и цезий самопроизвольно воспламеняются. Литий, натрий и калий хранят под слоем вазелина или вазелинового масла, рубидий и цезий хранят в запаянных ампулах. Металлы очень легкие и легкоплавкие, имеют довольно большой диапазон жидкого состояния. Щелочные металлы очень мягкие, натрий и калий легко режутся ножом.
Литий, натрий и калий весьма распространены в природе, образуют много самостоятельных минералов: LiAl(SiO 3) 2 - сподумен, LiAl(PO 4)F - амблигонит, NaCl галит (каменная или поваренная соль), Na 2 SO 4 10H 2 O - мирабилит, KCl - сильвин, NaClKCl - сильвинит, KClMgCl 2 6H 2 O - карналлит, КClMgSO 4 3H 2 O - каинит. Рубидий и цезий самостоятельных минералов не образуют, встречаются в виде примесей в минералах калия.
Литий и натрий получают электролизом ионных расплавов. Калий обычно получают восстановлением расплавов его соединений натрием или магнием.
Литий применяется в качестве легирующей добавки, придает сплавам твердость и пластичность. Натрий используется как теплоноситель в ядерных реакторах и восстановитель в металлотермии, а также как катализатор процессов полимеризации диенов. В лабораториях натрий широко используется для осушки газов и органических растворителей. Калий используется в промышленности как восстановитель и теплоноситель (в основном в виде жидкого сплава с натрием). Рубидий и цезий в основном применяются для изготовления фотоэлементов.
Химические свойства. Очень активные металлы, реагируют со всеми неметаллами, кроме инертных газов. Состав продуктов окисления кислородом зависит от природы металла: литий образует оксид, натрий и калий - перекисные соединения.
4Li + O 2 = 2Li 2 O; 2Na + O 2 = Na 2 O 2 ; K + O 2 = KO 2
пероксид натрия супероксид калия
С водой реагируют очень энергично, калий - со взрывом:
2K + 2H 2 O = 2KOH + H 2
Растворимы в аммиаке, с которым реагируют в присутствии катализатора:
2Na + 2NH 3 = 2NaNH 2 + H 2
Растворимы в ртути, образуя амальгамы, которые медленно разлагаются водой и используются в качестве мягкого восстановителя. Активно реагируют с оксидами, отбирая у них кислород, горят в атмосфере оксида углерода(IV):
4Na + SiO 2 = 2Na 2 O + Si; 4Li + CO 2 = 2Li 2 O + C
Свежая поверхность Э быстро темнеет вследствие образования оксидной пленки. Пленка эта относительно плотна - с течением времени весь металл медленно окисляется. Пленка состоит из ЭО, а также ЭО 2 и Э 3 N 2 . Нормальные электродные потенциалы реакций Э-2е = Э 2+ равны =-2,84В(Са), =-2,89(Sr). Э очень активные элементы: растворяются в воде и кислотах, вытесняют большинство металлов из их оксидов, галогенидов, сульфидов. Первично (200-300 о С) кальций взаимодействует с водяным паром по схеме:
2Са + Н 2 О = СаО + СаН 2 .
Вторичные реакции имеют вид:
CаН 2 + 2Н 2 О = Са(ОН) 2 + 2Н 2 и СаО + Н 2 О = Са(ОН) 2 .
В крепкой серной кислоте Э почти не растворяются ввиду образования пленки из малорастворимых ЭSO 4 . С разбавленными минеральными кислотами Э реагируют бурно с выделением водорода. Кальций при нагревании выше 800 о С с метаном реагирует по схеме:
3Cа + СН 4 = СаН 2 + СаС 2 .
Э при нагревании реагируют с водородом, с серой и с газообразным аммиаком. По химическим свойствам радий ближе всего к Ва, но он более активен. При комнатной температуре он заметно соединяется с кислородом и азотом воздуха. В общем, его химические свойства немного более выражены чем у его аналогов. Все соединения радия медленно разлагаются под действием собственного излучения, приобретая при этом желто-ватую или коричневую окраску. Соединения радия обладают свойством автолюминесценции. В результате радиоактивного распада 1 г Ra каждый час выделяет 553,7 Дж тепла. Поэтому температура радия и его соединений всегда выше температуры окружающей среды на 1,5 град. Также известно, что 1 г радия в сутки выделяет 1 мм 3 радона(226 Ra = 222 Rn + 4 He), на чем основано его применение как источника радона для радоновых ванн.
Гидриды Э - белые, кристаллические солеобразные вещества. Их получают непосредственно из элементов при нагревании. Температуры начала реакции Э + Н 2 = ЭН 2 равны 250 о С (Са), 200 о С (Sr), 150 о С (Ва). Термическая диссоциация ЭН 2 начинается при 600 о С. В атмосфере водорода СаН 2 не разлагается при температуре плавления (816 о С). В отсутствии влаги гидриды щелочноземельных металлов устойчивы на воздухе при обычной температуре. Они не реагируют с галогенами. Однако при нагревании химическая активность ЭН 2 возрастает. Они способны восстанавливать оксиды до металлов(W, Nb, Ti, Се, Zr, Ta), например
2СаН 2 + ТiO 2 = 2CaO + 2H 2 + Ti.
Реакция СаН 2 с Al 2 O 3 идет при 750 о С:
3СаН 2 + Al 2 O 3 = 3СаО + 3Н 2 + 2Аl,
СаН 2 + 2Al = CaAl 2 + H 2 .
С азотом СаН2 при 600оС реагирует по схеме:
3СаН 2 + N 2 = Ca 3 N 2 +3H 2 .
При поджигании ЭН 2 они медленно сгорают:
ЭН 2 + О 2 = Н 2 О + СаО.
В смеси с твердыми окислителями взрывоопасны. При действии воды на ЭН 2 выделяется гидроокись и водород. Эта реакция сильно экзотермична: смоченный водой на воздухе ЭН 2 самовоспламеняется. С кислотами ЭН 2 реагирует, например по схеме:
2HCl + CaH 2 = CaCl 2 + 2H 2 .
ЭН 2 применяют для получения чистого водорода, а также для определения следов воды в органических растворителях. Нитриды Э представляют собой бесцветные тугоплавкие вещества. Они получаются непосредственно из элементов при повышенной температуре. Водой они разлагаются по схеме:
Э 3 N 2 + 6H 2 O = 3Э(ОН) 2 + 2NH 3 .
Э 3 N 2 реагируют при нагревании с СО по схеме:
Э 3 N 2 + 3СО = 3ЭО + N 2 + 3C.
Процессы которые происходят при нагревании Э 3 N 2 с углем выглядят так:
Э3N2 + 5С = ЭCN2 + 2ЭС2; (Э = Са, Sr); Ва3N2 + 6С = Ва(СN)2 + 2ВаC2;
Нитрид стронция реагирует с HCl, давая хлориды Sr и аммония. Фосфиды Э 3 Р 2 образуются непосредственно из элементов или прокаливанием трехзамещенных фосфатов с углем:
Cа 3 (РО 4) 2 + 4С = Са 3 Р 2 + 4СО
Они гидролизуются водой по схеме:
Э 3 Р 2 + 6Н 2 О = 2РН 3 + 3Э(ОН) 2 .
С кислотами фосфиды щелочноземельных металлов дают соответствующую соль и фосфин. На этом основано их применение для получения фосфина в лаборатории.
Комплексные аммиакаты состава Э(NН 3) 6 - твердые вещества с металлическим блеском и высокой электропроводностью. Их получают действием жидкого аммиака на Э. На воздухе они самовоспламеняются. Без доступа воздуха они разлагаются на соответствующие амиды: Э(NH 3) 6 = Э(NH 2) 2 + 4NH 3 + Н 2 . При нагревании они энергично разлагаются по этой же схеме.
Карбиды щелочноземельных металлов которые получаются прокаливанием Э с углем разлагаются водой с выделением ацетилена:
ЭС 2 + 2Н 2 О = Э(ОН) 2 + С 2 Н 2 .
Реакция с ВаС 2 идет настолько бурно, что он воспламеняется в контакте с водой. Теплоты образования ЭС 2 из элементов для Са и Ва равны 14 и 12 ккалмоль. При нагревании с азотом ЭС 2 дают СаСN 2 , Ba(CN) 2 , SrCN 2 . Известны силициды (ЭSi и ЭSi 2). Их можно получить при нагревании непосредственно из элеменов. Они гидролизуются водой и реагируют с кислотами, давая H 2 Si 2 O 5 , SiH 4 , соответствующее соединение Э и водород. Известны бориды ЭВ 6 получаемые из элементов при нагревании.
Окиси кальция и его аналогов - белые тугоплавкие(T кип СаО = 2850 о С) вещества, энергично поглощающие воду. На этом основано применение ВаО для получения абсолютного спирта. Они бурно реагируют с водой, выделяя много тепла (кроме SrO растворение которой эндотермично). ЭО растворяются в кислотах и хлориде аммония:
ЭО + 2NH 4 Cl = SrCl 2 + 2NH 3 + H 2 O.
Получают ЭО прокаливанием карбонатов, нитратов, перекисей или гидроксидов соответствующих металлов. Эффективные заряды бария и кислорода в ВаО равны 0,86. SrO при 700 о С реагирует с цианистым калием:
KCN + SrO = Sr + KCNO.
Окись стронция растворяется в метаноле с образованием Sr(ОСН 3) 2 . При магнийтермическом восстановлении ВаО может быть получен промежуточный окисел Ва 2 О, который неустойчив и диспропорционирует.
Гидроокиси щелочноземельных металлов - белые растворимые в воде вещества. Они являются сильными основаниями. В ряду Са-Sr-Ba основной характер и растворимость гидроокисей увеличиваются. рПР(Са(ОН) 2) = 5,26, рПР(Sr(ОН) 2) = 3,5, рПР(Bа(ОН) 2) = 2,3. Из растворов гидроокисей обычно выделяются Ва(ОН) 2 . 8Н 2 О, Sr(ОН) 2 . 8Н 2 О, Cа(ОН) 2 . Н 2 О. ЭО присоединяют воду с образованием гидроокисей. На этом основано использование СаО в строительстве. Тесная смесь Са(ОН) 2 и NaOH в весовом соотношении 2:1 носит название натронная известь, и широко используется как поглотитель СО 2 . Са(ОН) 2 при стоянии на воздухе поглощает СО 2 по схеме:
Ca(OH)2 + CO2 = CaCO3 + Н2О.
Около 400 о С Са(ОН) 2 реагирует с угарным газом:
СО + Ca(OH) 2 = СаСО 3 + Н 2 .
Баритовая вода реагирует с СS 2 при 100 о С:
СS 2 + 2Ва(ОН) 2 = ВаСО 3 + Ва(НS) 2 + Н 2 О.
Алюминий реагирует с баритовой водой:
2Al + Ba(OH) 2 + 10H 2 O = Ba 2 + 3H 2 . Э(ОН) 2
используются для открытия угольного ангидрида.
Э образуют перекиси белого цвета. Они существенно менее стабильны в отличие от окисей и являются сильными окислителями. Практическое значение имеет наиболее устойчивая ВаО 2 , которая представляет собой белый, парамагнитный порошок с плотностью 4,96 г1см 3 и т. пл. 450°. BaО 2 устойчива при обычной температуре (может храниться годами), плохо растворяется в воде, спирте и эфире, растворяется в разбавленных кислотах с выделением соли и перекиси водорода. Термическое разложение перекиси бария ускоряют окислы, Cr 2 O 3 , Fe 2 O 3 и CuО. Перекись бария реагирует при нагревании с водородом, серой, углеродом, аммиаком, солями аммония, феррицианидом калия и т. д. С концентрированной соляной кислотой перекись бария реагирует, выделяя хлор:
ВаO 2 + 4НСl = BaCl 2 + Cl 2 + 2H 2 O.
Она окисляет воду до перекиси водорода:
Н 2 О + ВаО 2 = Ва(ОН) 2 + Н 2 О 2 .
Эта реакция обратима и в присутствии даже угольной кислоты равновесие смещено вправо. ВаО 2 используется как исходный продукт для получения Н 2 О 2 , а также как окислитель в пиротехнических составах. Однако, ВаО 2 может выступать и в качестве восстановителя:
HgCl 2 + ВаО 2 = Hg + BaCl 2 + O 2 .
Получают ВаО 2 нагреванием ВаО в токе воздуха до 500 о С по схеме:
2ВаО + О 2 = 2ВаО 2 .
При повышении температуры имеет место обратный процесс. Поэтому при горении Ва выделяется только окись. SrO 2 и СаО 2 менее устойчивы. Общим методом получения ЭО 2 является взаимодействие Э(ОН) 2 с Н 2 О 2 , при этом выделяются ЭО 2 . 8Н 2 О. Термический распад ЭО 2 начинается при 380 о С (Са), 480 о С (Sr), 790 о С (Ва). При нагревании ЭО 2 с концентрированной перекисью водорода могут быть получены желтые неустойчивые вещества -- надпероксиды ЭО 4 .
Соли Э как правило бесцветны. Хлориды, бромиды, иодиды и нитраты хорошо растворимы в воде. Фториды, сульфаты, карбонаты и фосфаты плохо растворимы. Ион Ва 2+ - токсичен. Галиды Э делятся на две группы: фториды и все остальные. Фториды почти не растворимы в воде и кислотах, и не образуют кристаллогидратов. Напротив хлориды, бромиды, и иодиды хорошо растворимы в воде и выделяются из растворов в виде кристаллогидратов. Некоторые свойства ЭГ 2 представлены ниже:
При получении путем обменного разложения в растворе фториды выделяются в виде объемистых слизистых осадков, довольно легко образующих коллоидные растворы. ЭГ 2 можно получить действуя соответствующими галогенами на соответствующие Э. Расплавы ЭГ 2 способны растворять до 30% Э. При изучении электропроводности расплавов хлоридов элементов второй группы главной подгруппы было установлено, что их молекулярно-ионный состав очень различен. Степени диссоциации по схеме ЭСl 2 = Э 2+ + 2Cl- равны: BeCl 2 - 0,009%, MgCl 2 - 14,6%, CaCl 2 - 43,3%, SrCl 2 - 60,6%, BaCl 2 - 80,2%. Галогениды (кроме фторидов) Э содержат кристаллизационную воду: CaCl 2 . 6Н 2 О, SrCl 2 . 6Н 2 О и ВаCl 2 . 2Н 2 О. Рентгеноструктурным анализом установлено строение Э[(ОН 2) 6 ]Г 2 для кристаллогидратов Са и Sr. При медленном нагревании кристаллогидратов ЭГ 2 можно получить безводные соли. CaCl 2 легко образует пересыщенные растворы. Природный СаF 2 (флюорит) применяют в керамической промышленности, а также он используется для производства HF и является минералом фтора. Безводный CaCl 2 используют как осушитель ввиду его гидроскопичности. Кристаллогидрат хлористого кальция используют для приготовления холодильных смесей. ВаСl 2 - используют в сх и для открытия
SO 4 2- (Ва 2+ + SO 4 2- = ВаSO 4).
Сплавлением ЭГ2 и ЭН2 могут быть получены гидрогалиды:
ЭГ 2 + ЭН 2 = 2ЭНГ.
Эти вещества плавятся без разложения но гидролизуются водой:
2ЭНГ + 2H 2 O = ЭГ 2 + 2Н 2 + Э(ОН) 2 .
Растворимость в воде хлоратов , броматов и иодатов в воде уменьшается по рядам Сa - Sr - Ba и Cl - Br - I. Ba(ClO 3) 2 - используется в пиротехнике. Перхлораты Э хорошо растворимы не только в воде но и в органических растворителях. Наиболее важным из Э(ClO 4) 2 является Ва(ClO 4) 2 . 3Н 2 О. Безводный перхлорат бария является хорошим осушителем. Его термический распад начинается только при 400 о С. Гипохлорит кальция Са(СlO) 2 . nH 2 O (n=2,3,4) получают действием хлора на известковое молоко. Он является окислителем и хорошо растворим в воде. Хлорную известь можно получить действуя хлором на твердую гашеную известь. Она разлагается водой и пахнет хлором в присутствии влаги. Реагирует с СО 2 воздуха:
СО 2 + 2CaOCl 2 = CаСO 3 + CaCl 2 + Cl 2 O.
Хлорная известь применяется как окислитель, отбеливатель и как дезинфицирующее средство.
Для щелочноземельных металлов известны азиды Э(N 3) 2 и роданиды Э(CNS) 2 . 3Н 2 О. Азиды по сравнению с азидом свинца гораздо менее взрывоопасны. Роданиды при нагревании легко теряют воду. Они хорошо растворимы в воде и органических растворителях. Ва(N 3) 2 и Ba(CNS) 2 могут быть использованы для получения азидов и роданидов других металлов из сульфатов обменной реакцией.
Нитраты кальция и стронция существуют обычно в виде кристаллогидратов Са(NO 3) 2 . 4H 2 O и Sr(NO 3) 2 . 4H 2 O. Для нитрата бария не свойственно образование кристаллогидрата. При нагревании Са(NO 3) 2 . 4H 2 O и Sr(NO 3) 2 . 4H 2 O легко теряю воду. В инертной атмосфере нитраты Э термически устойчивы до 455 o C (Са), 480 o C (Sr), 495 o C (Ba). Расплав кристаллогидрата нитрата кальция имеет кислую среду при 75 о С. Особенностью нитрата бария является малая скорость растворения его кристаллов в воде. Склонность к комплексообразованию проявляет лишь нитрат бария, для которого известен нестойкий комплекс K 2 . Нитрат кальция растворим в спиртах, метилацетате, ацетоне. Нитраты стронция и бария там же почти не растворимы. Температуры плавления нитратов Э оцениваются в 600 о С, однако при этой же температуре начинается распад:
Э(NO 3) 2 = Э(NO 2) 2 + O 2 .
Дальнейший распад идет при более высокой температуре:
Э(NO 2) 2 = ЭО + NO 2 + NO.
Нитраты Э уже издавна использовались в пиротехнике. Легколетучие соли Э окрашивают пламя в соответствующие цвета: Са - в оранжево-желтый, Sr - в красно-карминовый, Ba - в желто-зеленый. Разберемся в сущности этого на примере Sr: у Sr 2+ есть две ВАО: 5s и 5p или 5s и 4d. Сообщим энергию этой системе - нагреем. Электроны с более близлежащих к ядру орбиталей перейдут на эти ВАО. Но такая система не устойчива и выделит энергию в виде кванта света. Как раз Sr 2+ и излучает кванты с частотой, соответствующей длинам красных волн. При получении пиротехнических составов удобно использовать селитру, т.к. она не только окрашивает пламя, но и является окислителем, выделяя кислород при нагревании. Пиротехнические составы состоят из твердого окислителя, твердого восстановителя и некоторых органических веществ, обесцвечивающих пламя восстановителя, и являющихся связывающим агентом. Нитрат кальция используется как удобрение.
Все фосфаты и гидрофосфаты Э плохо растворимы в воде. Их можно получить растворением соответствующего количества СаО или СаСO 3 в ортофосфорной килоте. Также они осаждаются при обменных реакциях типа:
(3-х)Са 2+ + 2H x PO 4 -(3-х) = Са (3-х) (H x PO 4) 2 .
Практическое значение (как удобрение) имеет однозамещенный ортофосфат кальция, который наряду с Са(SO 4) входит в состав суперфосфата. Его получают по схеме:
Cа 3 (PO 4) 2 + 2H 2 SO 4 = Ca(H 2 PO 4) 2 + 2CаSO 4
Оксалаты тоже мало растворимы в воде. Практическое значение имеет оксалат кальция, который при 200 о С обезвоживается, а при 430 о С разлагается по схеме:
СаС 2 О 4 = СаСО 3 + СО.
Ацетаты Э выделяются в виде кристаллогидратов, и хорошо растворимы в воде.
Сульфаты Э - белые, плохо растворимые в воде вещества. Растворимость СaSO 4 . 2Н 2 О на 1000 г. воды при обычной температуре составляет 8 . 10 -3 моль, SrSO 4 - 5 . 10 -4 моль, ВаSO 4 - 1 . 10 -5 моль, RaSO 4 - 6 . 10 -6 моль. В ряду Са - Ra растворимость сульфатов быстро уменьшается. Ва 2+ является реактивом на сульфат-ион. Сульфат кальция содержит кристаллизационную воду. Выше 66 о С из раствора выделяется безводный сульфат кальция, ниже - гипс СаSO 4 . 2Н 2 О. Нагревание гипса выше 170 о С сопровождается выделением гидратной воды. При замешивании гипса с водой эта масса быстро твердеет вследствие образования кристал-логидрата. Это свойство гипса используется в строительстве. Египтяне использовали это знание еще 2000 лет назад. Растворимость ЭSO 4 в крепкой серной кислоте намного выше, чем в воде (ВаSO 4 до 10%), что свидетельствует о комплексообразовании. Соответствующие комплексы ЭSO 4 . Н 2 SO 4 могут быть получены в свободном состоянии. Двойные соли с сульфатами щелочных металлов и аммония известны только для Са и Sr. (NH 4) 2 растворим в воде и используется в аналитической химии для отделения Са от Sr, т.к. (NH 4) 2 мало растворим. Гипс применяют для комбинированного получения серной кислоты и цемента, т.к. при нагревании с восстановителем (углем) гипс разлагается:
СаSO 4 + С = СаО + SO 2 + СО.
При более высокой температуре (900 o C) сера еще больше восстанавливается по схеме:
СаSO 4 + 3С = СаS + CO 2 + 2СО.
Подобный распад сульфатов Sr и Ва начинается при более высоких температурах. ВаSO 4 нетоксичен и используется в медицине и производстве минеральных красок.
Сульфиды Э представляют собой белые твердые вещества, кристаллизующиеся по типу NaCl. Теплоты их образования и энергии кристаллических решеток равны (ккалмоль): 110 и 722 (Са), 108 и 687 (Sr), 106 и 656 (Ва). Могут быть получены синтезом из элементов при нагревании или прокаливанием сульфатов с углем:
ЭSO4 + 3С = ЭS + CO2 + 2СО.
Менее всех растворим СаS (0,2 гл). ЭS вступает в следующие реакции при нагревании:
ЭS + H 2 O = ЭO + H 2 S; ЭS + Г 2 = S + ЭГ 2 ; ЭS + 2O 2 = ЭSO 4 ; ЭS + xS = ЭS x+1 (x=2,3).
Сульфиды щелочноземельных металлов в нейтральном растворе нацело гидролизованы по схеме:
2ЭS + 2Н 2 О = Э(НS) 2 + Э(ОН) 2 .
Кислые сульфиды могут быть получены и в свободном состоянии упариванием раствора сульфидов. Они вступают в реакции с серой:
Э(НS) 2 + хS = ЭS x+1 + H 2 S (x=2,3,4).
Из кристаллогидратов известны ВаS . 6H 2 O и Са(HS) 2 . 6Н 2 О, Ва(HS) 2 . 4Н 2 О. Са(HS) 2 применяют для удаления волос. ЭS подвержены явлению фосфоресценции. Известны полисульфиды Э: ЭS 2 , ЭS 3 , ЭS 4 , ЭS 5 . Они получаются при кипячении взвеси ЭS в воде с серой. На воздухе ЭS окисляются: 2ЭS + 3О 2 = 2ЭSО 3 . Пропусканием воздуха через суспензию СаS можно получить тиосульфат Са по схеме:
2СаS + 2О 2 + Н 2 О = Са(ОН) 2 + СаS 2 О 3
Он хорошо растворим в воде. В ряду Са - Sr - Ва растворимость тиосульфатов падает. Теллуриды Э мало растворимы в воде и тоже подвержены гидролизу, но в меньшей степени чем сульфиды.
Растворимость хроматов Э в ряду Са - Ва падает также резко, как и в случае с сульфатами. Эти вещества желтого цвета получаются при взаимодействии растворимых солей Э с хроматами (или дихроматами) щелочных металлов:
Э 2+ + СrO 4 2- = ЭCrO4.
Хромат кальция выделяется в виде кристаллогидрата - СаCrO 4 . 2H 2 O (рПР СаCrO 4 = 3,15). Еще до температуры плавления он теряет воду. SrCrO 4 и ВаCrO 4 кристаллогидратов не образуют. pПР SrCrO 4 = 4,44, рПР ВаCrO 4 = 9,93.
Карбонаты Э белые, плохо растворимые в воде вещества. При нагревании ЭСО 3 переходят в ЭО, отщепляя СО 2 . В ряду Са - Ва термическая устойчивость карбонатов возрастает. Наиболее практически важен из них карбонат кальция (известняк). Он непосредственно используется в строительстве, а также служит сырьем для получения извести и цемента. Ежегодная мировая добыча извести из известняка исчисляется десятками миллионов тонн. Термическая диссоциация СаСО 3 эндотермична:
СаСО 3 = СаО + СО 2
и требует затраты 43 ккал на моль известняка. Обжиг СаСО 3 проводят в шахтных печах. Побочным продуктом обжига является ценный углекислый газ. СаО важный строительный материал. При замешивании с водой происходит кристаллизация за счет образования гидроокиси, а затем карбоната по схемам:
СаО + Н 2 О = Са(ОН) 2 и Са(ОН) 2 + СО 2 = СаСО 3 + Н 2 О.
Колоссально важную практическую роль играет цемент - зеленовато-серый порошок, состоящий из смеси различных силикатов и алюминатов кальция. Будучи замешан с водой он отвердевает за счет гидратации. При его производстве смесь СаСО 3 с глиной обжигают до начала спекания (1400-1500 о С). Затем смесь перемалывают. Состав цемента можно выразить процентным соотношением компонентов СаО, SiO 2 , Al 2 O 3 , Fe 2 O 3 , причем СаО представляет основание, а все остальное - ангидриды кислот. Состав силикатного (портладского) цемента слагается в основном из Са 3 SiO 5 , Ca 2 SiO 4 , Ca 3 (AlO 3) 2 и Ca(FeO 2) 2 . Его схватывание проходит по схемам:
Са 3 SiO 5 + 3Н 2 О = Ca 2 SiO 4 . 2Н 2 О + Са(ОН) 2
Ca 2 SiO 4 + 2Н 2 О = Ca 2 SiO 4 . 2Н 2 О
Ca 3 (AlO 3) 2 + 6Н 2 О = Ca 3 (AlO 3) 2 . 6Н 2 О
Ca(FeO 2) 2 + nH 2 O = Ca(FeO 2) 2 . nH 2 O.
Природный мел вводят в состав различных замазок. Мелкокристаллический, осажденный из раствора СаСО 3 входит в состав зубных порошков. Из ВаСО 3 прокаливанием с углем получают ВаО по схеме:
ВаСО 3 + С = ВаО + 2СО.
Если процесс вести при более высокой температуре в токе азота образуется цианид бария:
ВаСО 3 + 4С +N 2 = 3CO + Ba(CN) 2 .
Ва(СN) 2 хорошо растворим в воде. Ва(СN) 2 может использован для производства цианидов других металлов путем обменного разложения с сульфатами. Гидрокарбонаты Э растворимы в воде и могут быть получены лишь в растворе например, пропусканием углекислого газа в взвесь СаСО 3 в воде:
СО 2 + СаСО 3 + Н 2 О = Са(НСО 3) 2 .
Эта реакция обратима и при нагревании смещается влево. Наличие гидрокарбонатов кальция и магния в природных водах обуславливает жесткость воды.

